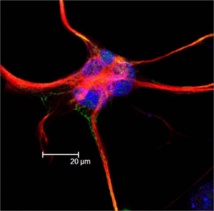
El cerebro obtiene su energía de una forma del azúcar, la glucosa, de manera muy eficiente. Sin embargo, dada la estructura del cerebro y las limitaciones metabólicas, la manera en que logra esta eficiencia es un misterio.
La clave radica en la relación –aún poco conocida- entre neuronas, vasos sanguíneos y otras células del cerebro, las células gliales. Científicos de la Escuela Politécnica Federal de Lausana (EPFL), en Suiza, y de la Universidad de Ciencia y Tecnología Rey Abdalá (KAUST) de Arabia Saudita han desarrollado el primer modelo computacional de esta relación, que encaja con datos obtenidos previamente en experimentos realizados in vivo e in vitro del cerebro.
Por otra parte, este modelo, publicado en PLOS Computational Biology, está siendo integrado en el Proyecto Blue Brain, cuyo objetivo es estudiar la estructura del cerebro de mamíferos creando una simulación de todo el cerebro a nivel molecular.
El modelo de un ‘trabajo en equipo’
En la página oficial de la EPFL se explica que el cerebro es más que neuronas que comparten información. De hecho, más de la mitad de este órgano en realidad está formado por las células gliales.
Estas células desempeñan, de forma principal, la función de soporte de las neuronas (les suministran energía y las protegen de los agentes patógenos, entre otras funciones); además de intervenir activamente en el procesamiento cerebral de la información en el organismo.
Así, las células gliales, las neuronas y los vasos sanguíneos del cerebro forman una unidad funcional, la llamada unidad vascular–neurona–glía (NGV, por sus siglas en inglés) que regula la gestión energética del cerebro.
De esta unidad es de lo que se ha logrado hacer un modelo computacional detallado, que captura con precisión su dinámica. Específicamente, el modelo muestra cómo se transporta la glucosa entre los tres elementos de la NGV para producir energía para las neuronas activadas.
El avance ha sido realizado por un equipo dirigido por Pierre Magistretti (EPFL, KAUST), con la colaboración de Renaud Jolivet (de la University College London, UCL).
Otros logros alcanzados
Experimentos previos realizados por Magistretti y su equipo habían mostrado que la glucosa fluye desde un tipo de células gliales llamadas «astrocitos» a las neuronas, en forma de lactato, un compuesto químico que desempeña importantes roles en varios procesos bioquímicos.
Sin embargo, algunos estudios teóricos habían propuesto que el lactato fluiría también en otra dirección – de las neuronas a los astrocitos-, lo que tendría importantes implicaciones para nuestra comprensión del metabolismo energético del cerebro.
El modelo ha confirmado ahora en términos cuantitativos los resultados de los experimentos de Magistretti: que el lactato fluye de los astrocitos a las neuronas. También ha simulado con éxito el tiempo que tarda este proceso; un avance que proporciona una imagen mensurable de cómo las neuronas y las células gliales coordinan el metabolismo energético cerebral.
Comprender el verdadero funcionamiento del cerebro
La comprensión de las relaciones metabólicas entre neuronas y células gliales tiene implicaciones importantes para la comprensión de las señales detectadas con técnicas de imagen cerebral, como la imagen por resonancia magnética funcional (fMRI) o la tomografía por emisión de positrones (PET), con las que se supervisa la utilización de glucosa, el flujo sanguíneo o los cambios en el consumo de oxígeno coincidentes con la actividad neuronal.
«Este es el primer modelo temporal y multi-escala de la unidad vascular-neurona-glía que refleja con precisión las observaciones experimentales de varios tipos de células y organismos», afirma Magistretti. «Al añadir la dinámica de las neuronas y las células gliales [al proyecto Blue Brain], podemos dar un paso hacia una modelización más precisa del verdadero funcionamiento del cerebro», concluye el investigador.
Referencia bibliográfica:
Jolivet R, Coggan JS, Allaman I, Magistretti PJ. Multi-timescale Modeling of Activity-Dependent Metabolic Coupling in the Neuron-Glia-Vasculature Ensemble. PLOS Computational Biology (2015). DOI: 10.1371/journal.pcbi.1004036.









Hacer un comentario