Una nueva tecnología desarrollada por investigadores de la Universidad de Bonn y la Universidad de California en Los Ángeles amplifica la visualización de la actividad neuronal mediante un sensor molecular.
La técnica muestra imágenes de alta resolución de las señales eléctricas en neuronas vivas, y al mismo tiempo desvela la cadena de luces que propaga la dinámica de las células nerviosas en el cerebro.
Según destacan los investigadores en una nota de prensa, la nueva técnica permitirá investigar cuestiones que antes estaban cerradas a la investigación científica en el campo de las neurociencias y hará posible comprender mejor el funcionamiento del cerebro. El trabajo ha sido publicado en la revista Proceedings of the National Academy of Sciences (PNAS).
Es indudable que en las últimas décadas los avances en cuanto a la comprensión de la actividad cerebral son notorios y abarcan diferentes campos de aplicación.
Hoy sabemos que las señales olfativas que entran en juego cuando apreciamos un perfume activan un grupo determinado de neuronas en un sector específico del cerebro. En tanto, los recuerdos que genera ese aroma se encuentran regulados por otras neuronas en otra región cerebral.
Sin embargo, todavía algunos de estos procesos y sus detalles permanecen ocultos para la ciencia, llevando a que los neurocientíficos desarrollen nuevos estudios. En esta ocasión, un grupo de científicos alemanes y estadounidenses ha logrado mejorar un método que permite amplificar la actividad neuronal y visualizarla al detalle.
Iluminar el cerebro
La tecnología, que optimiza desarrollos previos con enfoques similares, permite observar la función de las neuronas sin perturbarlas. De esta manera, es posible obtener una visión más precisa de las disfunciones asociadas a determinadas enfermedades neuronales.
Básicamente, la nueva técnica “ilumina” los procesos neuronales cuando se busca apreciarlos al detalle y con la máxima definición posible. Para ello aprovecha la tensión eléctrica que se genera a partir del contraste de la carga energética existente entre el interior y el exterior de las neuronas, que a su vez se transmite mediante los axones (extremidades de las células nerviosas) a modo de un “cableado” biológico.
Las diferencias en ese voltaje son aprovechadas por el nuevo sensor para iluminar la actividad neuronal, pero sin afectarla ni someterla a ninguna presión. Como resultado de la “iluminación”, el proceso deja al descubierto una cadena de luces alrededor de las células nerviosas. Mediante proteínas fluorescentes introducidas por modificaciones genéticas, los especialistas obtienen “marcadores” lumínicos que permiten rastrear la dinámica neuronal.
Mejoras y potencial a futuro
Aunque el método había sido desarrollado en investigaciones previas, el nuevo estudio logra mejorarlo considerablemente. Por ejemplo, extiende el lapso en el cual se mantiene la luminosidad en las zonas de acción del sensor, propiciando un mejor aprovechamiento de la técnica.
Además, el sensor reacciona más rápido y con mayor sensibilidad a los cambios más pequeños en las señales eléctricas producidas en las neuronas. De esta forma, permite visualizar y registrar hasta 100 pulsos eléctricos por segundo, ampliando considerablemente el potencial de estudio y análisis.
El nuevo enfoque también elimina compuestos potencialmente tóxicos que se empleaban en estudios previos para hacer visibles los cambios en la actividad neuronal. De esta forma, se garantiza que el proceso no impacte sobre la actividad de las neuronas mientras se llevan a cabo los estudios.
Sin duda, la posibilidad de optimizar la visualización de los procesos neuronales en células vivas es un avance científico con un enorme potencial y una gran cantidad de aplicaciones, como por ejemplo la detección de las anomalías que tienen lugar en las patologías neurodegenerativas o el reconocimiento de la forma precisa en la que actúa el cerebro frente a diferentes estímulos.
Referencia
A dark quencher genetically encodable voltage indicator (dqGEVI) exhibits high fidelity and speed. Therese C. Alich, Milan Pabst, Leonie Pothmann, Bálint Szalontai, Guido C. Faas and Istvan Mody. PNAS (2021).DOI:https://doi.org/10.1073/pnas.2020235118
Foto:
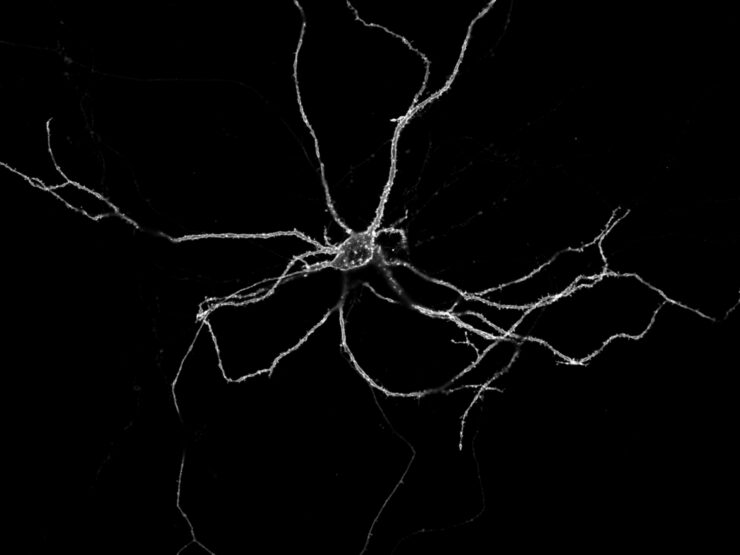
Imagen de una célula nerviosa viva cultivada en el laboratorio por los investigadores. La membrana que la rodea brilla intensamente porque la proteína fluorescente está en su exterior. Crédito: Milán Pabst.













Hacer un comentario