Un grupo de científicos del Whitehead Institute de Estados Unidos ha descubierto que cuando las células no pueden acceder a la suficiente cantidad de oxígeno para realizar sus funciones, una molécula denominada fumarato se activa: el “reemplazo” garantiza el flujo de energía hacia las células. Según los investigadores, el proceso identificado podría ser útil para desarrollar nuevos tratamientos contra enfermedades como diabetes, cáncer o isquemia, en las cuales se registra un fuerte descenso en los niveles de oxígeno en los tejidos.
La respiración celular es un proceso que se desarrolla en las mitocondrias y que facilita la creación de ATP, una molécula imprescindible para que nuestras células dispongan de la energía requerida para desarrollar sus funciones vitales. El mecanismo incluye múltiples reacciones encadenadas que concretan el transporte de electrones, en un “circuito” que culmina en la producción de ATP.
El oxígeno y la cadena de electrones
En el marco de este proceso, el oxígeno desempeña un papel de suma trascendencia, ya que en el paso final de las reacciones en cadena solamente se preservan dos electrones, los cuales se integran al oxígeno para completar el proceso. Es por ese motivo que dentro de este mecanismo se dice que el oxígeno funciona como un «aceptor terminal de electrones».
La función que cumple el oxígeno no solamente completa las reacciones, sino que además permite que el ciclo continúe con nuevos electrones “ingresando” en la cadena. Aunque ya se había observado que en determinadas ocasiones las células lograban mantener algunas funciones de la cadena de transporte de electrones, incluso en ausencia de oxígeno, no se había identificado hasta el momento cómo se concretaba ese proceso suplementario.
El “reemplazo” del oxígeno
De acuerdo a una nota de prensa, el grupo de científicos liderado por la investigadora principal Jessica Spinelli se propuso entender cómo son capaces las mitocondrias de mantener todo el proceso, cuando el oxígeno no cumple la función de aceptor de electrones terminal. Según lo indicado en el nuevo estudio, publicado recientemente en la revista Science, una molécula llamada fumarato interviene en casos de escasez de oxígeno y funciona como aceptor terminal de electrones: gracias a esto, la función mitocondrial es posible en este entorno.
Los especialistas ya sabían que el fumarato se utiliza como aceptor de electrones en organismos eucariotas inferiores, pero las características del proceso son claramente diferentes: se usa una enzima y un portador de electrones que no poseen los mamíferos. Por lo tanto, era imprescindible hallar otros elementos para poder explicar el desarrollo de este mecanismo en el caso de los mamíferos.
A través de una serie de ensayos y experimentos con roedores, los investigadores pudieron determinar que la clave se encontraba en la acumulación de una molécula llamada ubiquinol, que los científicos comprobaron que se concentraba en condiciones de bajo oxígeno o hipoxia. Es precisamente la molécula ubiquinol la que invierte y modifica ciertos procesos que tienen lugar en el complejo de proteínas SDH: las modificaciones “liberan” al fumarato para que pueda llevar adelante su papel definitorio en la cadena de transporte de electrones.
Tema relacionado: Crean un tejido sintético en el que crecen vasos sanguíneos.
Tejidos más receptivos
Un punto clave de la investigación es que los científicos apreciaron que los tejidos reaccionaban de forma diferente en los roedores: el riñón, el hígado y el cerebro lograban casi la misma eficacia en la función mitocondrial con el fumarato reemplazando al oxígeno. Por el contrario, tejidos como el corazón y el músculo esquelético llevaban adelante el proceso con fumarato, pero sin retener con la misma eficacia la función mitocondrial cuando el oxígeno era mínimo.
En consecuencia, el descubrimiento podría conducir al desarrollo de nuevas terapias y tratamientos en patologías que generan una reducción de oxígeno a nivel celular, sobre todo cuando se ven afectados los tejidos y órganos que muestran una mayor respuesta al proceso de “reemplazo” mediante el fumarato.
Referencia
Fumarate is a terminal electron acceptor in the mammalian electron transport chain. Jessica B. Spinelli, Paul C. Rosen, Hans-Georg Sprenger, Anna M. Puszynska, Jessica L. Mann, Julian M. Roessler, Andrew L. Cangelosi, Antonia Henne, Kendall J. Condon, Tong Zhang, Tenzin Kunchok, Caroline A. Lewis, Navdeep S. Chandel and David M. Sabatini. Science (2021). DOI:https://doi.org/10.1126/science.abi7495
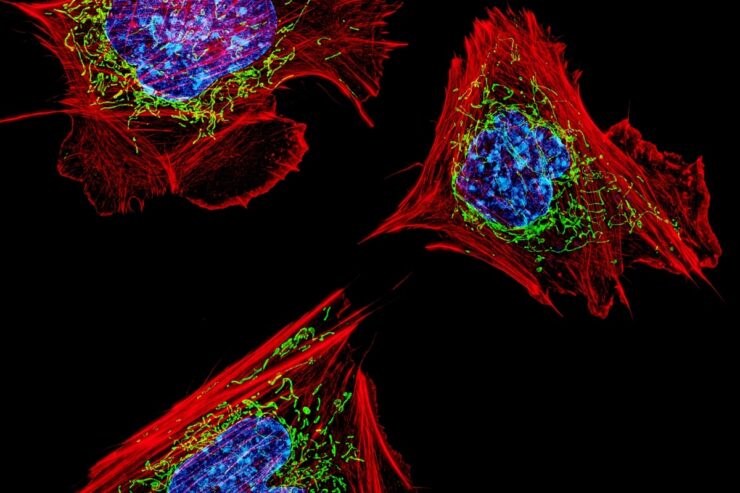
Foto: células de ratón con mitocondrias en verde, núcleos en azul y el citoesqueleto de actina en rojo. Créditos: Dylan Burnette and Jennifer Lippincott-Schwartz, Eunice Kennedy Shriver National Institute of Child Health and Human Development, National Institutes of Health. Part of the exhibit Life:Magnified by ASCB and NIGMS. Licensed under CC BY-NC-ND 2.0













Hacer un comentario