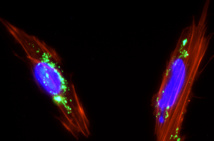
Las células madre mesenquimales, capaces de diferenciarse en varios tipos de células, se localizan en diferentes partes del cuerpo humano, como la placenta.
Una de sus características es que tienen capacidad migratoria, es decir, que pueden viajar hacia lugares donde se haya producido una inflamación, al detectar las quimioquinas generadas por estos tejidos inflamados.
“Las células mesenquimales descubren esta sobreexpresión y migran hacia los lugares con inflamación donde se diferenciarán en tejido conectivo, para contrarrestar la alteración del tejido”, explica María Vallet-Regí, catedrática de Química Inorgánica y Bioinorgánica de la Universidad Complutense de Madrid y miembro del Centro de Investigación Biomédica en Red de Bioingeniería, Biomateriales y Nanomedicina (CIBER-BBN).
En colaboración con el Grupo de Medicina Regenerativa del Instituto de Investigación Hospital 12 de Octubre (Madrid), los científicos han utilizado estas células para que, insertándoles nanopartículas de sílice cargadas con un fármaco antitumoral, lleguen a tumores mamarios, donde existe inflamación celular.
“Estamos utilizando a las células mesenquimales de placenta como transporte de nuestras nanopartículas. Esa capacidad de traslado hacia tumores de pecho la hemos estudiado tanto in vitro como in vivo, y hemos observado que las nanopartículas llegan a su objetivo gracias a estos fantásticos vehículos celulares”, afirma Ana Isabel Flores, responsable del Grupo de Medicina Regenerativa y coautora del trabajo.
El estudio, publicado en Acta Biomaterialia, contempla dos modelos, uno con líneas celulares de laboratorio (in vitro) y el otro con ratas (in vivo). En ambos, los investigadores han demostrado que las nanopartículas mesoporosas de sílice no son tóxicas para las células madre de placenta y que no afectan a su capacidad migratoria.
Un proceso rápido y eficaz
Los científicos han conseguido que el proceso de insertar las nanopartículas en las células sea rápido y eficiente (de unas dos horas) y han logrado que estas se queden en su interior durante largos períodos de tiempo (como mínimo, cinco días).
“También hemos demostrado que podemos cargar un citotóxico (doxorrubicina) habitualmente empleado como fármaco antitumoral en nuestras nanopartículas y que, tras introducirlas en las células de la placenta, provocan la muerte de células tumorales in vitro”, subraya otro de los coautores el estudio, Miguel Manzano, investigador del departamento de Química Inorgánica y Bioinorgánica de la UCM y miembro de CIBER-BBN.
El proceso se basa en cultivar células mesenquimales de placenta en el laboratorio sobre las que se añaden las nanopartículas previamente preparadas y modificadas para favorecer su internalización.
“Las condiciones de carga no pueden ser muy agresivas porque necesitamos mantener con vida a las células transportadoras”, destaca Vallet-Regí, autora principal del estudio. Por eso, los investigadores tuvieron que fijar la concentración de nanopartículas que podían usar, modificaron su superficie para favorecer su internalización y evaluaron los tiempos óptimos necesarios.
“Una vez que los parámetros han sido optimizados, es un proceso relativamente sencillo”, comenta la científica.
Células sin dilema ético
Entre las principales ventajas del sistema está que, al atacar directamente al tumor, se evitan los efectos secundarios de una terapia antitumoral convencional. Además, se duplica el efecto, puesto que a la capacidad destructora de tumores de este tipo de células se le añade la del fármaco que viaja a bordo de la nanopartícula.
Los científicos también destacan que utilizar estas células no implica ningún dilema ético, como sí ocurre con las células madre embrionarias. “Como provienen de un adulto (la madre) que da su consentimiento, no plantean ningún tipo de conflicto ético”, recalca Flores.
Utilizar estas células, localizadas en las placentas de mujeres que han dado a luz y que han solicitado que se almacenen en hospitales como el 12 de Octubre, no requiere usar ninguna técnica agresiva, lo que elimina cualquier riesgo para la donante, destacan los autores.
Referencia bibliográfica:
Juan L. Paris, Paz de la Torre, Miguel Manzano, M. Victoria Cabañas, Ana I. Flores y María Vallet-Regí. Decidua-derived mesenchymal stem cells as carriers of mesoporous silica nanoparticles. In vitro and in vivo evaluation on mammary tumors. Acta Biomaterialia (2016). DOI: 10.1016/j.actbio.2016.01.017.













Hacer un comentario