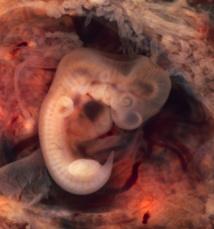
Uno de los principales mecanismos que emplea el organismo para protegerse del cáncer es apagar células defectuosas volviéndolas senescentes: estas células no mueren, pero dejan de dividirse; su ciclo vital se para.
Un estudio coordinado por el CNIO (Centro Nacional de Investigaciones Oncológicas) con la colaboración de la Universidad Autónoma de Barcelona ha descubierto que la senescencia ocurre como parte del desarrollo embrionario normal de los mamíferos y no sólo como respuesta a un daño en las células.
El estudio ha sido publicado en Cell junto a un segundo trabajo desarrollado por el Centre de Regulació Genòmica (CRG) en torno al mismo proceso biológico.
Senescencia también durante el desarrollo embrionario
La senescencia celular determina la parada del ciclo celular y está implicada en los procesos en los que se produce daño celular: además de para frenar el cáncer, sucede también durante el envejecimiento. El trabajo, dirigido por Manuel Serrano, investigador del CNIO, demuestra ahora que este proceso biológico se produce también durante el desarrollo embrionario de los mamíferos.
El estudio, en que han colaborado los investigadores de la UAB Jesús Ruberte (CBATEG y Departamento de Sanidad y Anatomía Animal) y Alfonso Rodríguez-Baeza (Departamento de Ciencias Morfológicas, Área de anatomía y Embriología Humana), pone de manifiesto que durante la degeneración del mesonefros, un riñón embrionario transitorio, y la formación del oído interno, la senescencia celular contribuye a la remodelación de estos órganos. A medida que el embrión crece y sus tejidos van cambiando de forma y función, la senescencia apaga células que ya no son necesarias.
Desde un punto de vista mecanístico, la senescencia embrionaria es dependiente del gen p21, pero independiente de p53 o del daño del DNA, y está regulada por las vías TGF-ß/SMAD y PI3K/FOXO. Posteriormente, los tejidos embrionarios son infiltrados por los macrófagos, que eliminan las células senescentes, lo que permite la reorganización de los tejidos y la formación de los órganos definitivos del adulto.
Conceptualmente, este estudio añade la senescencia celular a la lista de procesos claves que contribuyen al desarrollo embrionario, tales como la proliferación, la diferenciación, la migración y la muerte celular.
También abre la posibilidad a la hipótesis de que la senescencia celular apareciera durante la evolución como un mecanismo capaz de remodelar los órganos embrionarios, y que posteriormente en el periodo adulto, se haya adaptado para regenerar los tejidos dañados, señala una nota de prensa de la UAB.
Los bomberos y el fuego
La senescencia se presenta, a menudo como un arma de doble filo: a la vez que protege del cáncer, tiene un papel importante en el envejecimiento del organismo. Sin embargo, el trabajo presentado ahora alerta contra la idea simplista de que el envejecimiento es consecuencia de la senescencia.
«En mi opinión, la senescencia es un proceso fundamentalmente beneficioso porque su objetivo es eliminar células dañadas en adultos», explica Serrano en un comunicado del CNIO.
«Lo que ocurre es que cuando envejecemos hay más daños celulares y por lo tanto más senescencia». En otras palabras, atribuir a las senescencia la causa del envejecimiento es como atribuir a los bomberos la causa de los incendios porque siempre están ellos cuando se produce uno.
Los investigadores del CNIO han trabajado con embriones de ratón y también humanos, mientras que los del CRG han trabajado con embriones de pollo y de ratón, con resultados similares entre especies.
Referencias bibliográficas:
Daniel Muños-Espín, Marta Cañamero, Antonio Maraver, Gonzalo Gómez-López, Julio Contreras, Silvia Murillo-Cuesta, Alfonso Rodríguez-Baeza, Isabel Varela-Nieto, Jesús Ruberte, Manuel Collado, Manuel Serrano. Programmed cell senescence during mammalian embryonic development. Cell (2013). DOI: http://dx.doi.org/10.1016/j.cell.2013.10.019.
Mekayla A. Storer et. al. Senescence Is a Developmental Mechanism that Contributes to Embryonic Growth and Patterning. Cell (2013). DOI: http://dx.doi.org/10.1016/j.cell.2013.10.041














Hacer un comentario